|
目前,过渡金属催化的酮类化合物的不对称转移氢化是制备手性醇的有效策略。使用半三明治结构的Ru/Rh催化剂,一系列芳基/烷基、炔基/烷基、全氟烷基/烷基取代的酮以及α-酮酯或α-酮酰胺已可以被氢化并以较高的ee值得到手性醇。
α-手性硼酸酯是有机合成、药物化学和材料科学中有用的合成单元。酰基硼酸酯作为方便易得的前手性羰基化合物,被广泛应用于酰胺合成、杂环形成及交叉偶联反应等。然而,该类化合物的催化不对称转化尚未实现。
近期,中国科学院福建物质结构研究所房新强课题组在温和条件下实现了酰基硼酸酯的不对称转移氢化。一系列含芳基、烷基、炔基、烯基以及羰基的酰基硼类底物均能够进行反应并以优异的对映选择性得到产物。产物中极具价值的硼基单元能够进行一系列官能团转化,并得到传统不对称转移氢化难以得到的醇类产物以及天然产物和药物分子。DFT计算阐明了N-甲基亚氨基二乙酸硼酯在羰基分子的不对称转移氢化中优越的导向作用。上述成果将启发通过导向基团的合理使用以实现不对称转移氢化过程中选择性的精准控制的研究工作。
相关研究成果发表在《美国化学会志》(JACS)上。该工作由福建物构所和合肥工业大学合作完成。研究工作得到国家自然科学基金、中国科学院战略性先导科技专项、福建省自然科学基金的支持。
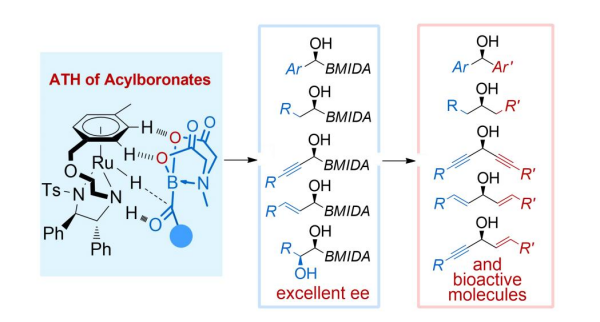
酰基硼的不对称转移氢化 |
